
พัฒนาสมรรถนะของวิธีการหาปริมาณไนโตรเจนในเดกซ์แทรนด้วยวิธี Kjeldahl
ศักรินทร์ วรรณวงศ์
สำนักเครื่องมือวิทยาศาสตร์และการทดสอบ มหาวิทยาลัยสงขลานครินทร์ อำเภอหาดใหญ่ จังหวัดสงขลา 90110
(อีเมลผู้ประพันธ์บรรณกิจ: [email protected])
Received: 12 January 2026, Revised: 18 February 2026, Accepted: 20 February 2026, Published: 23 February 2026
บทคัดย่อ
เดกซ์แทรน (Dextran) เป็นพอลิแซ็กคาไรด์จากธรรมชาติที่มีความสำคัญและใช้งานหลากหลายทั้งในด้านการแพทย์ งานวิจัย และอุตสาหกรรม เนื่องจากมีความปลอดภัยสูง ละลายน้ำได้ดี และสามารถปรับคุณสมบัติได้ตามน้ำหนักโมเลกุล เดกซ์แทรนมีโครงสร้างทางเคมีที่ประกอบด้วยคาร์บอน ไฮโดรเจน และออกซิเจน หากมีการตรวจพบไนโตรเจนในเดกซ์แทรนจึงบ่งชี้ถึงสิ่งเจือปนที่ตกค้างจากกระบวนการผลิต เช่น โปรตีนหรือเศษเซลล์จุลินทรีย์ ซึ่งในบางกรณีอาจส่งผลให้เกิดการแพ้หรืออาการไม่พึงประสงค์อื่น ๆ การควบคุมและตรวจวิเคราะห์ไนโตรเจนรวมจึงมีความสำคัญต่อการประเมินความบริสุทธิ์ คุณภาพ และความปลอดภัยของผลิตภัณฑ์ โดยเฉพาะการใช้งานทางการแพทย์ งานวิจัยนี้มีวัตถุประสงค์เพื่อพัฒนาสมรรถนะของวิธี Kjeldahl สำหรับการหาปริมาณไนโตรเจนในเดกซ์แทรน ด้วยเครื่อง Nitrogen Analyzer (Kjeltec™ 8400, FOSS, เดนมาร์ก) ในปัจจุบันมีการทดสอบหาปริมาณไนโตรเจนตกค้างในผลิตภัณฑ์เดกซ์แทรน หรือ พอลิแซ็กคาไรด์ (Polysaccharide) อื่น ๆ แต่ยังไม่พบงานวิจัยที่มุ่งเน้นการตรวจสอบความใช้ได้ของวิธีตามหลักการ Method validation ของตัวอย่างประเภทดังกล่าว ได้แก่ ความเป็นเส้นตรง (Linearity) ขีดจำกัดการตรวจวัด (LOD) ขีดจำกัดการหาปริมาณ (LOQ) ความถูกต้อง (Accuracy) และความเที่ยง (Precision) ผลการวิจัยพบว่าช่วงการทดสอบคือ 25 - 500 mg N/kg โดยมีค่า LOD เท่ากับ 15 mg N/kg และ LOQ เท่ากับ 50 mg N/kg การประเมิน Intermediate Precision โดยผู้วิเคราะห์ 2 คน ต่างวันและเวลา ไม่มีความแตกต่างอย่างมีนัยสำคัญทางสถิติ (t = –0.704, p > 0.05) สรุปได้ว่าวิธี Kjeldahl ที่ใช้สำหรับทดสอบตัวอย่างเดกซ์แทรน มีความเหมาะสม ถูกต้อง สามารถใช้เป็นวิธีมาตรฐานสำหรับการควบคุมคุณภาพและความปลอดภัยของผลิตภัณฑ์เดกซ์แทรนได้
คำสำคัญ: เดกซ์แทรน; พอลิแซ็กคาไรด์; ไนโตรเจน; วิธี Kjeldahl; การตรวจสอบความใช้ได้ของวิธี; ความเป็นเส้นตรง; ความถูกต้อง; ความเที่ยง
Development and Performance Validation of the Kjeldahl Method for Nitrogen Determination in Dextran
Sakkarin Wannawong
Office of Scientific Instrument and Testing, Prince of Songkla University, Hat Yai District, Songkhla 90110, Thailand
(Corresponding author’s e-mail: [email protected])
Abstract
Dextran is a naturally derived polysaccharide with wide-ranging applications in medical, research, and industrial fields due to its high safety, excellent water solubility, and tunable properties depending on molecular weight. Chemically, dextran consists solely of carbon, hydrogen, and oxygen. Therefore, the detection of nitrogen in dextran indicates the presence of impurities remaining from the production process, such as proteins or microbial cell residues, which in some cases may cause allergic reactions or other adverse effects. Consequently, the control and determination of total nitrogen content are essential for assessing the purity, quality, and safety of dextran products, particularly for medical applications. This study aimed to develop and evaluate the performance of the Kjeldahl method for the determination of nitrogen content in dextran using a Nitrogen Analyzer (Kjeltec™ 8400, FOSS, Denmark). Although nitrogen residue analysis has been reported for dextran and other polysaccharide products, no previous studies have specifically focused on validating the analytical method according to standard method validation principles for this type of sample. The validation parameters evaluated included linearity, limit of detection (LOD), limit of quantification (LOQ), accuracy, and precision. The results demonstrated good method performance over a concentration range of 25 - 500 mg N/kg, with an LOD of 15 mg N/kg and an LOQ of 50 mg N/kg. Intermediate precision evaluated by two analysts on different days and times showed no statistically significant difference between analysts (t = –0.704, p > 0.05). In conclusion, the Kjeldahl method developed for dextran analysis is suitable, accurate, and precise, and can be applied as a standard method for quality control and safety assessment of dextran products.
Keywords: Dextran; Polysaccharide; Nitrogen; Kjeldahl method; Method validation; Linearity; Accuracy; Precision
บทนำ
เดกซ์แทรนเป็นพอลิแซ็กคาไรด์ที่สังเคราะห์จากซูโครสโดยแบคทีเรียกรดแลคติก (Lactic Acid Bacteria) มีมวลโมเลกุลขนาดต่างกันไปตามเทคนิคการสังเคราะห์ ส่งผลให้คุณสมบัติของเดกซ์แทรนมีความหลากหลาย เช่น การละลายน้ำ ความหนืด และการเปลี่ยนแปลงเนื่องจากความร้อน (Díaz-Montes, 2021) รวมทั้งความเข้ากันได้ทางชีวภาพ ซึ่งไม่ก่อให้เกิดการตอบสนองทางภูมิคุ้มกัน (Lanvers et al., 2025) ปัจจุบันจึงมีการประยุกต์ใช้ในหลายสาขา ทั้งทางการแพทย์ เภสัชกรรม และอุตสาหกรรมทางด้านอาหาร จากการที่ผลิตภัณฑ์เดกซ์แทรนมีการบริโภคหรือสัมผัสโดยตรงกับร่างกายมนุษย์ การควบคุมคุณภาพและความปลอดภัยของผลิตภัณฑ์จึงมีความสำคัญอย่างยิ่ง (Ministry of Health, Labour and Welfare, 2016) โดยเฉพาะการควบคุมสิ่งเจือปนที่อาจตกค้างจากกระบวนการผลิต หนึ่งในตัวชี้วัดสำคัญคือปริมาณไนโตรเจนตกค้าง ซึ่งสามารถสะท้อนถึงการมีโปรตีนหรือสารอินทรีย์อื่น ๆ ที่ยังหลงเหลืออยู่ในผลิตภัณฑ์ สิ่งเจือปนเหล่านี้สามารถส่งผลกระทบต่อคุณภาพและความปลอดภัยของผลิตภัณฑ์ และในบางกรณีอาจก่อให้เกิดปฏิกิริยาภูมิแพ้หรืออาการไม่พึงประสงค์อื่น ๆ ดังนั้น การวิเคราะห์และควบคุมปริมาณไนโตรเจนจึงเป็นองค์ประกอบสำคัญของระบบประกันคุณภาพ โดยเฉพาะในห้องปฏิบัติการวิเคราะห์ด้วยเครื่องวิเคราะห์หาปริมาณไนโตรเจน ภายใต้การดำเนินงานของสำนักเครื่องมือวิทยาศาสตร์และการทดสอบ ซึ่งเป็นหน่วยงานที่มีการพัฒนาระบบคุณภาพอย่างต่อเนื่องตามมาตรฐานสากล และมีบทบาทสำคัญในการสนับสนุนการตรวจวิเคราะห์ที่ถูกต้องและเชื่อถือได้สำหรับผลิตภัณฑ์ที่เกี่ยวข้องกับความปลอดภัยของผู้บริโภค
วิธี Kjeldahl เป็นเทคนิคมาตรฐานที่ได้รับการยอมรับอย่างแพร่หลาย สำหรับการหาปริมาณไนโตรเจนในตัวอย่างชีวภาพ อาหาร และสิ่งแวดล้อม ในการวิจัยนี้ได้มีการดัดแปลงวิธี Kjeldahl มาตรฐานตามแนวทางของ (Ministry of Health, Labour and Welfare, 2016) เพื่อให้เหมาะสมกับเครื่องมือวิเคราะห์ที่มีอยู่ในหน่วยงาน และสอดคล้องกับลักษณะของตัวอย่างเดกซ์แทรน ซึ่งจำเป็นต้องวิเคราะห์ปริมาณไนโตรเจนในระดับความเข้มข้นต่ำ แตกต่างจากตัวอย่างของแข็งทั่วไป เช่น ดิน ปุ๋ย ชีวมวลฯ โดยเฉพาะอย่าง
ยิ่ง อาหารและวัตถุดิบอาหารที่มีไนโตรเจนเป็นองค์ประกอบหลักทางเคมี มีการพัฒนาและประยุกต์ใช้รูปแบบ Micro-Kjeldahl อย่างต่อเนื่อง เพื่อลดปริมาณสารเคมี ลดเวลาการย่อย และเพิ่มความไวของการตรวจวัด โดยยังคงความถูกต้องและความเที่ยงของผลวิเคราะห์ให้อยู่ในเกณฑ์ที่ยอมรับได้ตามแนวทาง AOAC และระบบคุณภาพห้องปฏิบัติการ (นิภาภรณ์ ลักษณ์สมยา และจินตนา กิจเจริญวงศ์, 2015) ซึ่งแตกต่างจากพอลิแซ็กคาไรด์เชิงบริสุทธิ์ที่มีปริมาณของไนโตรเจนที่ต่ำ การวิเคราะห์ปริมาณไนโตรเจนตกค้างจึงมีความท้าทายเฉพาะด้าน ทั้งในแง่ของประสิทธิภาพการย่อยสลายด้วยกรด ความไวของการตรวจวัด และผลกระทบจากเมทริกซ์ที่มีคาร์โบไฮเดรตเป็นองค์ประกอบหลัก การนำวิธี Kjeldahl ที่พัฒนาขึ้นสำหรับเมทริกซ์ทั่วไปมาใช้โดยตรงกับเดกซ์แทรนโดยไม่มีการตรวจสอบความเหมาะสมของวิธี อาจนำไปสู่ความคลาดเคลื่อนของผลการวิเคราะห์และส่งผลต่อการประเมินคุณภาพของผลิตภัณฑ์ ด้วยเหตุนี้จึงมีการปรับเปลี่ยนความเข้มข้น ปริมาณ และชนิดของ รีเอเจนต์ที่ใช้ในการวิเคราะห์ เพื่อให้เหมาะสมกับตัวอย่างประเภทพอลิแซ็กคาไรด์ชนิดนี้
แม้ว่าในปัจจุบันจะมีการนำวิธี Dumas (Combustion Method) มาใช้ในการวิเคราะห์ไนโตรเจนเพิ่มขึ้น แต่ด้วยข้อจำกัดของวิธี Dumas ที่ให้ขีดจำกัดการตรวจวัดค่อนข้างสูงกว่า (Thompson et al., 2002) และการใช้ปริมาณตัวอย่างน้อยซึ่งอาจไม่สะท้อนความเป็นตัวแทนของตัวอย่างทั้งหมด (Beljkaš et al., 2010) ทั้งยังเป็นเครื่องมือที่มีราคาแพงและต้นทุนค่าใช้จ่ายสูง ทำให้วิธี Kjeldahl ยังคงเป็นวิธีหลักที่เหมาะสมสำหรับการบริการทดสอบตัวอย่างในห้องปฏิบัติการของสำนักเครื่องมือวิทยาศาสตร์และ การทดสอบ โดยเฉพาะในบริบทของการให้บริการแก่ภาคอุตสาหกรรมและหน่วยงานกำกับดูแล อย่างไรก็ตาม จากการทบทวนวรรณกรรมยังไม่พบรายงานการศึกษาที่มุ่งเน้นการตรวจสอบความถูกต้องของวิธี Kjeldahl สำหรับการวิเคราะห์ปริมาณไนโตรเจนในเมทริกซ์ของเดกซ์แทรนโดยเฉพาะ ทั้งในแง่ของสมรรถนะของวิธีและความเหมาะสมต่อการใช้งานเชิงบริการทดสอบ ซึ่งเป็นช่องว่างทางวิชาการและเชิงมาตรฐานที่สำคัญ เนื่องจากการขาดข้อมูลการตรวจสอบความถูกต้องของวิธีในเมทริกซ์ดังกล่าว อาจจำกัดการยอมรับผลการวิเคราะห์ในระดับอุตสาหกรรมและการอ้างอิงตามระบบคุณภาพสากล
ดังนั้น การศึกษาครั้งนี้จึงมีวัตถุประสงค์เพื่อพัฒนาและประเมินสมรรถนะของวิธี Kjeldahl สำหรับการหาปริมาณไนโตรเจนในเดกซ์แทรน โดยดำเนินการตรวจสอบพารามิเตอร์สำคัญของการตรวจสอบความถูกต้องของวิธี (Method Validation) ได้แก่ ความเป็นเส้นตรง (Linearity) ขีดจำกัดการตรวจวัด (Limit of Detection, LOD) ขีดจำกัดการหาปริมาณ (Limit of Quantitation, LOQ) ความถูกต้อง (Accuracy) และความเที่ยง (Precision) ผลการศึกษาที่ได้ ไม่เพียงยืนยันความเหมาะสมของวิธี Kjeldahl สำหรับเมทริกซ์เดกซ์แทรนเท่านั้น แต่ยังมีความสำคัญเชิงอุตสาหกรรมและเชิงมาตรฐาน ในการสนับสนุนการจัดทำวิธีทดสอบอ้างอิง การควบคุมคุณภาพผลิตภัณฑ์ และการให้บริการวิเคราะห์ภายใต้ระบบคุณภาพตามมาตรฐานสากลของห้องปฏิบัติการทดสอบ
วัตถุประสงค์การศึกษา
เพื่อพัฒนาสมรรถนะของวิธี Kjeldahl ในการหาปริมาณไนโตรเจนในเดกซ์แทรนและการตรวจสอบความใช้ได้ของวิธี
วิธีการศึกษา
เครื่องมือ
ดำเนินการย่อยตัวอย่างด้วยระบบย่อยอัตโนมัติ ประกอบด้วยเครื่องย่อย (DT 2520, FOSS, เดนมาร์ก) และชุดกำจัดไอกรด (Scrubber 2501, FOSS, เดนมาร์ก) สำหรับการหาปริมาณไนโตรเจน ใช้เครื่องกลั่น (Kjeltec™ 8400, FOSS, เดนมาร์ก) ที่ติดตั้งอุปกรณ์ป้อนตัวอย่างอัตโนมัติ (Kjeltec™ Sampler 2420, FOSS, เดนมาร์ก) โดยมีระบบหล่อเย็นด้วยน้ำ (CA-1116A, EYELA, ญี่ปุ่น) ในกระบวนการกลั่น
สารเคมีและสารมาตรฐาน
ขั้นตอนการย่อยตัวอย่างใช้เม็ดย่อยตัวเร่งปฏิกิริยา ซึ่งประกอบด้วยโพแทสเซียมซัลเฟต (K₂SO₄) น้ำหนัก 3.5 กรัม และคอปเปอร์(II) ซัลเฟตเพนตาไฮเดรต (CuSO₄·5H₂O) น้ำหนัก 0.4 กรัม (Kjeltec™, FOSS) 1‑ออคทานอล (PanReac) กรดซัลฟิวริกเข้มข้น 95 - 97% (Merck) และสารละลายไฮโดรเจนเปอร์ออกไซด์ 30% (Sigma-aldrich) สำหรับขั้นตอนการกลั่น ใช้สารละลายโซเดียมไฮดรอกไซด์ 50% (AGC VINYTHAI) ส่วนในขั้นตอนการไทเทรต สารเคมีที่ใช้ประกอบด้วย กรดไฮโดรคลอริก 37% (Lab Scan) เอทานอล (Lab Scan) บรอมโครซอลกรีน (Lab Scan) กรดโบริก (Merck) และเมทิลเรด (PanReac) และสำหรับการตรวจสอบความถูกต้องของวิธี (Method Validation) ใช้สารมาตรฐาน ได้แก่ Acetanilide (Sigma-Aldrich) Amido Sulfuric Acid (Merck) และ Ammonium Sulfate (Loba)
วิธีการทดสอบ
1) การเตรียมตัวอย่างและสารมาตรฐาน
อบแห้งตัวอย่าง ที่อุณหภูมิ 103 ± 2 °C ข้ามคืน ทิ้งไว้อุณหภูมิห้องในโถดูดความชื้น รอวิเคราะห์ ก่อนการวิเคราะห์ สำหรับการตรวจสอบความใช้ได้ของวิธี เตรียมสารละลายมาตรฐาน Amidosulfonic acid ในน้ำ DI ให้มีความเข้มข้นของไนโตรเจน อยู่ที่ 202.32 mg N/L ใช้ในการ Spike เข้าสู่เมทริกซ์ตัวอย่างที่ความเข้มข้นต่างๆ เพื่อยืนยันความถูกต้องและความเที่ยงของวิธี
2) การหาปริมาณไนโตรเจนด้วยวิธี Kjeldahl
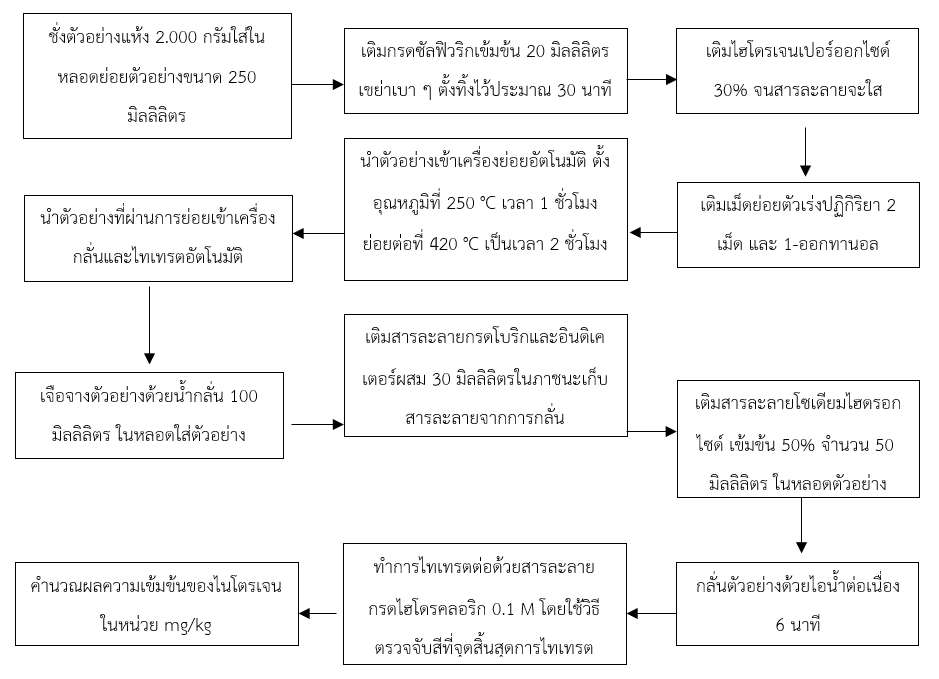
ภาพที่ 1 แผนผังกระบวนการวิเคราะห์ปริมาณไนโตรเจนรวมในตัวอย่างเดกซ์แทรนด้วยวิธี Kjeldahl
3) การตรวจสอบความใช้ได้ของวิธี
(1) ความเป็นเส้นตรง (Linearity)
ปิเปตสารละลายมาตรฐาน Amido Sulfuric Acid ลงในตัวอย่างเดกซ์แทรน ให้ได้ความเข้มข้นสุดท้าย 25 50 100 200 และ 500 mg N/kg จากนั้นนำไปทดสอบและเขียนกราฟระหว่างปริมาณของไนโตรเจนที่เตรียม กับปริมาณของไนโตรเจนที่วัดได้ คำนวณค่าสัมประสิทธิ์สหสัมพันธ์ (Correlation Coefficient, r) เพื่อศึกษาความเป็นเส้นตรง
(2) ขีดจำกัดการตรวจวัด (LOD) ขีดจำกัดการหาปริมาณ (LOQ)
การประเมินค่า LOD และ LOQ ทำโดยการใช้ตัวอย่างทดสอบตัวอย่างที่มีความเข้มข้นของไนโตรเจนในปริมาณที่ต่ำหรือใกล้ศูนย์ แล้วทำการทดสอบโดยใช้ตัวอย่างเดกซ์แทรนที่ปราศจากไนโตรเจน มาเติมสารละลายมาตรฐาน Amido Sulfuric Acid ให้ได้ความเข้มข้น 25 mg N/kg จำนวน 7 ซ้ำ เพื่อนำไปคำนวณหาค่า LOD และประมาณค่าของ LOQ ซึ่งคำนวณได้จากสมการ (Cantwell, 2025)
LOD=3×s0’
LOQ=10×s0’
โดยที่ s0’=s0 × √ (1/n + 1/nb)
s0 คือ ส่วนเบี่ยงเบนมาตรฐานของผลการทดสอบ m ซ้ำที่ความเข้มข้นต่ำ
s0’ คือ ส่วนเบี่ยงเบนมาตรฐานเพื่อใช้คำนวณ LOD และ LOQ
n คือ จำนวนการวิเคราะห์ซ้ำสำหรับการทดสอบประจำ
nb คือ จำนวนแบลงค์สำหรับการทดสอบประจำ
เมื่อได้ค่าประมาณจากการคำนวณ LOQ แล้ว ทำการทดสอบยืนยันโดยเตรียมตัวอย่างและเติมสารมาตรฐานลงในตัวอย่างที่ระดับค่าประมาณ LOQ จำนวน 7 ซ้ำ วิเคราะห์ปริมาณไนโตรเจน แล้วคำนวณร้อยละการได้กลับคืน (%Recovery) และ ร้อยละส่วนเบี่ยงเบนมาตรฐานสัมพัทธ์ (%RSD) เพื่อหาค่า LOQ ที่มีความถูกต้องและความเที่ยงที่ยอมรับได้
(3) การทดสอบความถูกต้อง (Precision) และความถูกต้อง (Accuracy)
ทดสอบความถูกต้องและความเที่ยงของวิธีวิเคราะห์ โดยเติมสารละลายมาตรฐาน Amido Sulfuric Acid ลงในตัวอย่าง ที่ผ่านกระบวนการเตรียมตัวอย่างตามขั้นตอน ให้ได้ความเข้มข้นสุดท้าย 3 ระดับละ คือ 50 100 และ 500 mg N/kg ระดับละ 7 ซ้ำโดยที่ระดับ 50 mg N/kg คือ ระดับ LOQ วิเคราะห์หาปริมาณไนโตรเจน คำนวณค่าเฉลี่ยร้อยละของการคืนกลับ (% Recovery) และค่าร้อยละของค่าเบี่ยงเบนมาตรฐานสัมพัทธ์ (%Relative Standard Deviation, %RSD) นอกจากนี้ยังมีการทำ Intermediate Precision โดย เตรียมตัวอย่างเช่นเดียวกันโดยผู้ทดสอบ 2 คน ทดสอบต่างวัน ด้วยเครื่องมือเดิม ทำคนละ 5 ซ้ำ คำนวณ %RSD ค่าเฉลี่ย %Recovery พร้อมทั้งเปรียบเทียบความต่างของผลการทดสอบของผู้วิเคราะห์
ผลการศึกษา
ความเป็นเส้นตรง (Linearity)
วิเคราะห์ความเป็นเส้นตรง ในช่วง 25 ถึง 500 mg N/kg โดยเขียนกราฟระหว่างปริมาณของไนโตรเจนในตัวอย่างที่เตรียม กับปริมาณของไนโตรเจนในตัวอย่างที่วัดได้ โดยกราฟมีความเป็นเส้นตรงตลอดช่วงที่ทดสอบ โดยมีค่าสัมประสิทธิ์สหสัมพันธ์ (Correlation Coefficient, r) เท่ากับ 0.999 (ภาพที่ 1)
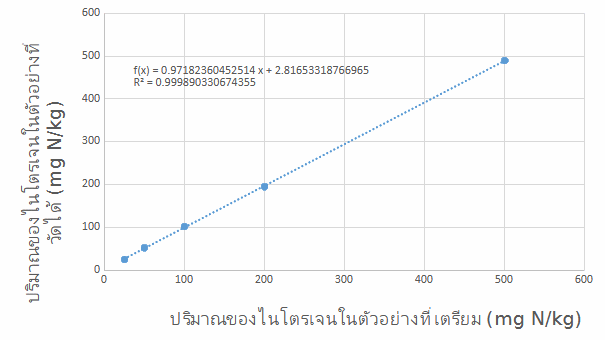
ภาพที่ 2 กราฟแสดงความสัมพันธ์ระหว่างความเข้มข้นของไนโตรเจนในตัวอย่างที่เตรียม (mg N/kg) กับความเข้มข้นของไนโตรเจนในตัวอย่างที่วัดได้ (mg N/kg)
ขีดจำกัดการตรวจวัด (LOD) ขีดจำกัดการหาปริมาณ (LOQ)
จากผลการวิเคราะห์ค่า LOD อยู่ที่ 15 mg N/kg และ LOQ อยู่ที่ 50 mg N/kg ยืนยันด้วยการเติมสารละลาย
มาตรฐาน Amido sulfuric acid ลงในตัวอย่างให้ได้ความเข้มข้นสุดท้าย 50 mg N/kg จำนวน 7 ซ้ำ ได้ค่าเฉลี่ย %Recovery และ (%RSD) ดังแสดง (ตารางที่1)
ตารางที่ 1 ผลการวิเคราะห์หาค่า LOD LOQ และผลการทดสอบความเที่ยงและความถูกต้องที่ระดับความเข้มข้น 50 mg N/kg
(ระดับ LOQ)
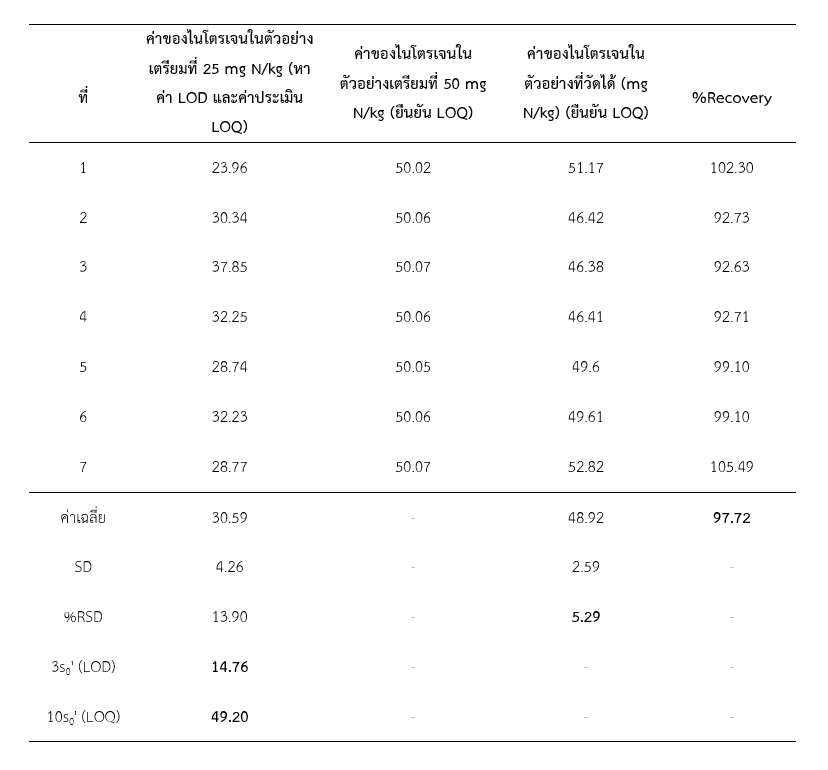
การทดสอบความถูกต้องและความเที่ยง
การทดสอบความถูกต้องและความเที่ยง โดยการเติมสารละลายมาตรฐานในตัวอย่างเดกซ์แทรนที่ระดับ 100 และ 500 mg N/L เพื่อให้ครอบคลุมช่วงการทดสอบ คือ ช่วงต่ำ (50 mg N/kg: LOQ) ช่วงกลาง (100 mg N/kg) และ ช่วงสูง (500 mg N/kg) โดยที่ระดับ 100 mg N/kg และ 500 mg N/kg ได้ค่าเฉลี่ย %Recovery และ %RSD ดังแสดง (ตารางที่2)
ตารางที่ 2 ผลการทดสอบความถูกต้องและความเที่ยงของการวิเคราะห์หาปริมาณไนโตรเจนในตัวอย่างเดกซ์แทรนที่ระดับ 100 mg N/kg และ 500 mg N/kg
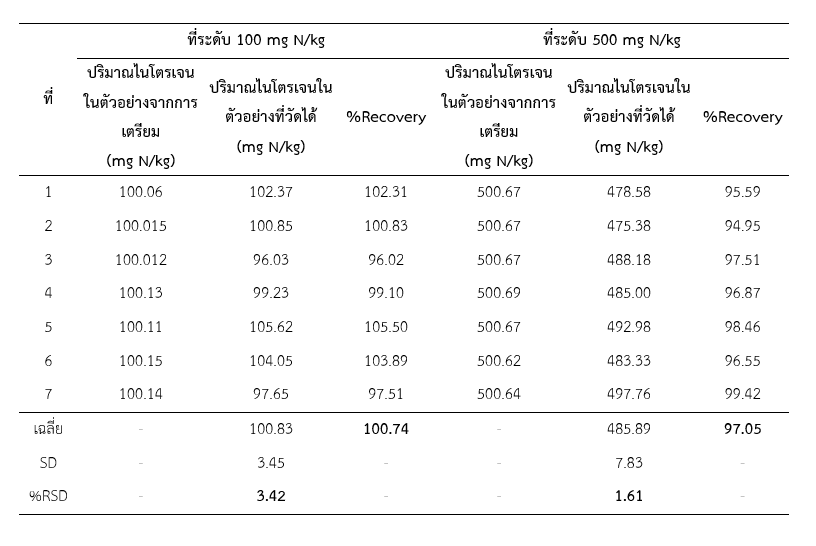
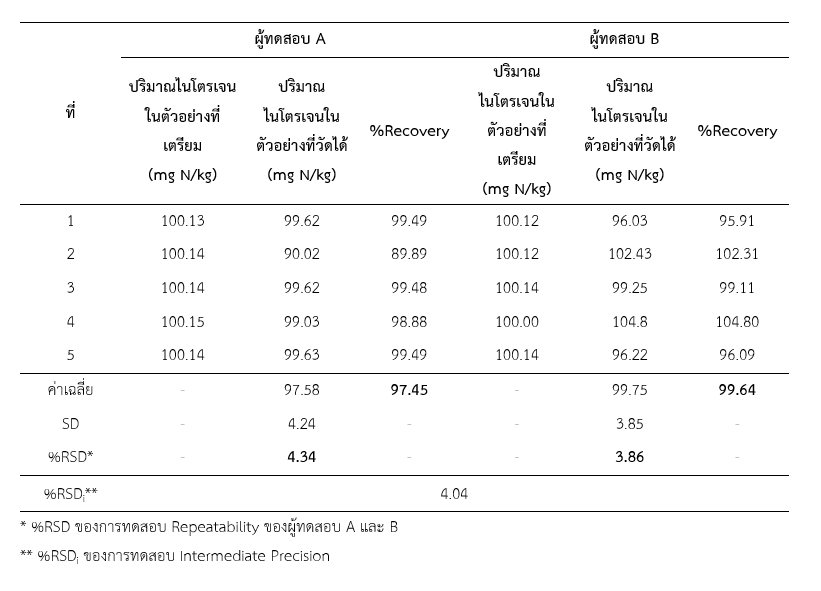
ผลการศึกษา Intermediate Precision โดยผู้ทดสอบ 2 คน ต่างวันและเวลา ทดสอบด้วยวิธีและเครื่องมือเดียวกัน ตัวอย่างจำนวน 5 ซ้ำต่อผู้ทดสอบ ได้ผล %RSD %RSDi และ %Recovery (ตารางที่ 3) เมื่อทำการเปรียบเทียบค่าเฉลี่ยด้วยสถิติ t-test ได้ค่า t = –0.704 (p > 0.05) ซึ่งมีค่าน้อยกว่าค่า t-critical ที่ df = 4 ที่ระดับนัยสำคัญ 95% คือ 2.776
ตารางที่ 3 ผลการทดสอบความเที่ยงและความถูกต้องของการทดสอบ Intermediate Precision
อภิปรายผลการศึกษา
แม้ว่าวิธี Kjeldahl จะเป็นวิธีมาตรฐานที่ได้รับการยอมรับอย่างกว้างขวาง แต่จากกลไกของวิธีพบว่ามีหลายปัจจัยที่อาจก่อให้เกิดความคลาดเคลื่อนของผลการวิเคราะห์ได้ โดยเฉพาะเมื่อประยุกต์ใช้กับตัวอย่างที่มีปริมาณไนโตรเจนต่ำมาก ในขั้นตอนการย่อย (Digestion) ความสมบูรณ์ของการเปลี่ยนไนโตรเจนอินทรีย์ให้เป็นแอมโมเนียมซัลเฟตถือเป็นปัจจัยสำคัญ หากอุณหภูมิ เวลา หรือปริมาณตัวเร่งปฏิกิริยาไม่เหมาะสม อาจทำให้การย่อยไม่สมบูรณ์ ส่งผลให้ค่าที่วัดได้ต่ำกว่าความเป็นจริง (Negative Bias) นอกจากนี้ วิธี Kjeldahl แบบดั้งเดิมไม่สามารถวัดไนโตรเจนในรูป Nitrate หรือ Nitrite ได้โดยตรง หากมีอยู่ในตัวอย่างโดยไม่ได้ผ่านขั้นตอนรีดักชันเพิ่มเติม จะทำให้ผลวิเคราะห์ต่ำกว่าปริมาณไนโตรเจนรวมจริง ขั้นตอนการกลั่น (Distillation) ประสิทธิภาพของการดักจับแอมโมเนียมีผลโดยตรงต่อความถูกต้องของผลวิเคราะห์ การสูญเสียแอมโมเนียระหว่างการกลั่นหรือการกลั่นไม่สมบูรณ์จะทำให้ผลการทดสอบผิดพลาดได้ สำหรับขั้นตอนการไทเทรต ความถูกต้องของสารมาตรฐานและการกำหนดจุดยุติ (Endpoint) มีผลต่อ Systematic Error ของวิธี หากสารมาตรฐานไม่ได้ทำการปรับมาตรฐานความเข้มข้นอย่างถูกต้อง อาจทำให้ผลการวิเคราะห์เบี่ยงเบนทั้งระบบได้
อย่างไรก็ตาม วิธี Kjeldahl ถูกเลือกใช้ในการวิเคราะห์ปริมาณไนโตรเจนในเดกซ์แทรน เนื่องจากเป็นวิธีมาตรฐานที่ได้รับการยอมรับในระดับสากล สำหรับการหาปริมาณไนโตรเจนในตัวอย่างอินทรีย์ แม้จะมีเทคนิคทางเลือก เช่น Combustion Method แต่ Kjeldahl มีความเหมาะสมกับลักษณะของเดกซ์แทรน ซึ่งเป็น Polysaccharide ที่มีปริมาณไนโตรเจนต่ำมาก โดยวิธีดังกล่าวมีความจำเพาะต่อไนโตรเจนอินทรีย์ และสามารถควบคุมสภาวะการทดสอบได้อย่างมีประสิทธิภาพ ส่งผลให้มีความเหมาะสมสำหรับการประเมินไนโตรเจนในระดับความเข้มข้นต่ำ เพื่อการควบคุมคุณภาพผลิตภัณฑ์ ซึ่งปัจจุบันมีการหาปริมาณไนโตรเจนในตัวอย่างประเภทเดกซ์แทรนหรือโพลิแซ็กคาไรด์อื่น ๆ ด้วยวิธี Kjeldahl (Cheng et al., 2017; Tarr & Hibbert, 1931) แต่ยังไม่พบงานที่มุ่งตรวจสอบความใช้ได้ของวิธีอย่างเป็นระบบในตัวอย่างกลุ่มนี้โดยตรง งานวิจัยนี้จึงทำการพัฒนาสมรรถนะของวิธีการวิเคราะห์ดังกล่าวผ่านตัวชี้วัดสำคัญ ได้แก่ Linearity เพื่อทำการประเมินความเป็นเส้นตรงตลอดช่วงการทดสอบ, ขีดจำกัดการวัด (LOD)และขีดจำกัดการวัดเชิงปริมาณ (LOQ) เพื่อประเมินขีดความสามารถของวิธีในการหาปริมาณไนโตรเจนในตัวอย่างเดกซ์แทรนที่ความเข้มข้นต่ำ โดยต้องน้อยกว่าเกณฑ์การยอมรับของไนโตรเจนในเดกซ์แทรน และต้องมีความถูกต้อง (Accuracy) และความเที่ยง (Precision) รวมถึง Intermediate Precision ในส่วนของความเที่ยง พิจารณา %RSD ซึ่งอยู่ในระดับต่ำ แสดงถึงความสม่ำเสมอของผลการวิเคราะห์เมื่อทำการทดสอบซ้ำภายใต้สภาวะเดียวกัน ค่าดังกล่าวบ่งชี้ว่าวิธีมีความเที่ยง (Repeatability) ที่ดี และมีความแปรปรวนภายในชุดการทดลองอยู่ในระดับที่ยอมรับได้ เช่นเดียวกันความถูกต้องที่พิจารณาจากค่าเฉลี่ย %Recovery สะท้อนให้เห็นว่าวิธีวิเคราะห์สามารถวัดปริมาณไนโตรเจนในตัวอย่างได้ใกล้เคียงกับค่าจริง (AOAC International, 2023; ICH, 2005; Cantwell, 2025)
จากการตรวจสอบความใช้ได้ของวิธีการวิเคราะห์หาปริมาณไนโตรเจนในตัวอย่างเดกซ์แทรนด้วยวิธี Kjeldahl พบว่าการทดสอบในช่วง 25 ถึง 500 mg N/kg มีความเป็นเส้นตรง โดยช่วงที่เลือกนำมาใช้ครอบคลุม เกณฑ์ปริมาณไนโตรเจนที่ยอมให้มีได้ไม่เกิน 100 mg/kg โดยเลือกช่วงที่ 25% 50% 100% ของเกณฑ์ (ICH, 2005) เพื่อวัดประสิทธิภาพต่ำสุดของการตรวจวัด ประสิทธิภาพต่ำสุดของการตรวจวัดเชิงปริมาณ ประสิทธิภาพการตรวจวัดที่ความเข้มข้นเท่ากับเกณฑ์การยอมรับ ตามลำดับ และช่วง 200% 500% ของเกณฑ์การยอมรับ เพื่อพิสูจน์พฤติกรรมตัวอย่างที่มีไนโตรเจนที่ความเข้มข้นสูงยังให้ผลการทดสอบที่น่าเชื่อถือหรือไม่ ซึ่งจากการทดสอบพบว่ามีค่าสัมประสิทธิ์สหสัมพันธ์เท่ากับ 0.999 ซึ่งมากกว่าเกณฑ์ที่ยอมรับได้อยู่ที่มากกว่า 0.995 (ICH, 2005)
จากการทดสอบหาขีดจำกัดของการวัด พบว่าในทางทฤษฎีสามารถคำนวณค่า LOD ผ่านการทดสอบ Blank ได้ แต่ในทางปฏิบัติจริงผลของ LOD สูงเกินเกณฑ์ ดังนั้นจึงทำการประเมิน LOD โดยการเติมสารมาตรฐานลงในตัวอย่างให้ได้ความเข้มข้นต่ำๆ เป็นจำนวน 7 ซ้ำ คำนวณค่า LOD และค่าประมาณ LOQ เมื่อได้ค่าประมาณของ LOQ จากนั้นได้ทดสอบความถูกต้องและความเที่ยงเป็นจำนวน 7 ซ้ำ โดยทั่วไปการประเมินความแม่นยำของวิธีวิเคราะห์ควรใช้จำนวนซ้ำอย่างน้อย 6 ซ้ำตามแนวทางสากล เพื่อให้การประมาณค่าความแปรปรวนมีความน่าเชื่อถือ ในการศึกษานี้จึงเลือกใช้ 7 ซ้ำ เพื่อเพิ่มเสถียรภาพของค่าทางสถิติและลดความไม่แน่นอน และค่า Outlier ของผลการทดสอบ ผลของค่าเฉลี่ย %Recovery 97.72 ซึ่งทั้งหมดอยู่ในเกณฑ์ที่ยอมรับได้ คือร้อยละ 90 - 107 สำหรับ%RSD ที่ระดับ LOQ พบว่ามีค่าเท่ากับ 5.29 ซึ่งอยู่ในเกณฑ์ที่ยอมรับได้เช่นกัน คือ ไม่มากกว่า 5.3 (AOAC International, 2023) ซึ่งค่า LOQ ที่ระดับ 50 mg N/kg มีความถูกต้องและน่าเชื่อถือ ค่า LOQ ที่ได้มีค่าต่ำกว่าข้อกำหนดสูงสุดของผลิตภัณฑ์อย่างชัดเจน ซึ่งอยู่ที่ร้อยละ 0.01 หรือ 100 mg N/kg แสดงให้เห็นว่าวิธีวิเคราะห์มีความไวเพียงพอสำหรับการควบคุมคุณภาพผลิตภัณฑ์ ทั้งนี้การที่ LOQ ต่ำกว่าระดับเกณฑ์ยอมรับมาก ยังสะท้อนถึงศักยภาพของวิธีในการตรวจติดตามการปนเปื้อนในระดับต่ำได้อย่างมีประสิทธิภาพ และมีความเหมาะสมสำหรับการใช้งานในเชิงอุตสาหกรรม นอกจากที่ระดับ LOQ แล้วยังได้ทดสอบความถูกต้องและความเที่ยงในช่วง 100 mg N/kg และ 500 mg N/kg เพิ่มเติม เพื่อยืนยันว่าทั้งช่วงการทดสอบมีความเหมาะสม ผลคือมีค่าเฉลี่ย %Recovery 100.74 และ 97.75 ตามลำดับ ซึ่งอยู่ในช่วงเกณฑ์การยอมรับคือ 90 - 107 และ 95 - 105 ตามลำดับ %RSD คือ 3.42 และ 1.64 ตามลำดับ ค่าที่ได้ไม่มากกว่าเกณฑ์การยอมรับคือ 5.3 และ 3.7 ตามลำดับ (AOAC International, 2023) เมื่อเปลี่ยนผู้ทดสอบ โดยทดสอบต่างวันและเวลากัน พบว่า %RSDi ของการทดสอบอยู่ที่ 4.04 ซึ่งพบว่าต่ำกว่าเกณฑ์การยอมรับ คือ 8 (AOAC International, 2023) และเมื่อนำผลของผู้ทดสอบมาเปรียบเทียบความต่างโดยใช้ค่าทางสถิติ t-test พบว่าผลการทดสอบของผู้ทดสอบทั้งสองไม่ได้ต่างกันอย่างมีนัยสำคัญ ดังนั้นจึงสรุปได้ว่าการทดสอบหาปริมาณไนโตรเจนในตัวอย่างดังกล่าว สามารถใช้งานได้ตลอดทั้งช่วงการทดสอบ และมีความถูกต้อง
จากการนำวิธีที่ผ่านการยืนยันสมรรถนะแล้วไปประยุกต์ใช้กับตัวอย่างเดกซ์แทรนเชิงพาณิชย์ พบว่าไม่ตรวจพบไนโตรเจนหรือโปรตีนตกค้างจากกระบวนการผลิต โดยมีค่าต่ำกว่า LOD และเป็นไปตามข้อกำหนดของ Japanese Pharmacopoeia แสดงให้เห็นว่าผลิตภัณฑ์มีความปลอดภัยในด้านการปนเปื้อนของสารไนโตรเจนจากแหล่งชีวภาพ ในเชิงการนำไปใช้ งานวิจัยนี้ให้กรอบวิธีวิเคราะห์ที่ผ่านการรับรองสมรรถนะครบถ้วน ซึ่งสามารถนำไปใช้เป็น วิธีมาตรฐานของสำนักเครื่องมือวิทยาศาสตร์และการทดสอบ สำหรับการให้บริการทดสอบเดกซ์แทรนและโพลิแซ็กคาไรด์ที่ใช้ในอุตสาหกรรมยา อาหาร และเวชภัณฑ์ โดยช่วยสนับสนุน การควบคุมคุณภาพวัตถุดิบและผลิตภัณฑ์สำเร็จรูป การตรวจรับรองตามข้อกำหนดเภสัชตำรับ และการประเมินความสอดคล้องของกระบวนการผลิต (Process Verification)
งานวิจัยนี้สามารถใช้เป็นต้นแบบในการพัฒนาและขยายขอบเขตการให้บริการของสำนักเครื่องมือวิทยาศาสตร์และการทดสอบไปยังโพลิแซ็กคาไรด์หรือสารชีวพอลิเมอร์ชนิดอื่นที่มีลักษณะเมทริกซ์ใกล้เคียงกัน โดยใช้กรอบการประเมินสมรรถนะเดียวกัน งานวิจัยนี้ไม่เพียงยืนยันความเหมาะสมของวิธี Kjeldahl สำหรับการวิเคราะห์ไนโตรเจนในเดกซ์แทรนในเชิงวิชาการเท่านั้น แต่ยังมีคุณค่าเชิงปฏิบัติในการสนับสนุนภารกิจหลักของสำนักเครื่องมือวิทยาศาสตร์และการทดสอบ ทั้งในด้านการให้บริการทดสอบ การควบคุมคุณภาพ และการสร้างความเชื่อมั่นให้กับผู้ใช้บริการและภาคอุตสาหกรรมที่เกี่ยวข้อง
สรุปผลการศึกษา
วิธีการวิเคราะห์หาปริมาณไนโตรเจนในตัวอย่างเดกซ์แทรน โดยวิธี Kjeldahl พบว่ามีความเป็นเส้นตรงในช่วง 25 ถึง 500 mg N/kg โดยขีดจำกัดการตรวจวัด (LOD) เท่ากับ 15 mg N/kg และขีดจำกัดการตรวจวัดเชิงปริมาณ (LOQ) เท่ากับ 50 mg N/kg การทดสอบความถูกต้องและความเที่ยงของวิธี ผลการทดสอบอยู่ผ่านเกณฑ์การยอมรับของ AOAC รวมทั้ง Intermediate Precision ที่ทดสอบตัวอย่างโดยผู้ทดสอบ 2 คน ต่างวันและเวลา พบว่าผลการทดสอบไม่ต่างกันอย่างมีนัยสำคัญ และ ร้อยละของค่าเบี่ยงเบนมาตรฐานสัมพัทธ์ อยู่ในเกณฑ์ที่ยอมรับได้ จึงสรุปได้ว่าการทดสอบหาปริมาณไนโตรเจนในตัวอย่างดังกล่าว สามารถใช้งานได้ตลอดทั้งช่วงการทดสอบ และมีความถูกต้อง ทั้งยังใช้วิธีมาตรฐานของสำนักเครื่องมือวิทยาศาสตร์และการทดสอบ สำหรับการให้บริการทดสอบเดกซ์แทรนและโพลิแซ็กคาไรด์ได้ ซึ่งจากการทดสอบหาการปนเปื้อนของไนโตรเจนหรือโปรตีนที่ตกค้างระหว่างกระบวนการผลิตของเดกซ์แทรน พบว่าตัวอย่างยังคงตรวจไม่พบการปนเปื้อนดังกล่าว นั้นคือมีค่าต่ำกว่า LOD ซึ่งผ่านเกณฑ์ที่ยอมให้มีได้ไม่เกินร้อยละ 0.01 ตามเกณฑ์ Japanese Pharmacopoeia แสดงว่าผลิตภัณฑ์เหล่านี้มีความปลอดภัยจากการตกค้างของไนโตรเจนจากกระบวนการผลิต อย่างไรก็ตาม นอกเหนือจากควบคุมปริมาณไนโตรเจนแล้ว ยังมีการควบคุมคุณภาพในด้านอื่น ๆ เช่น Antigenicity โลหะหนัก คลอไรด์ เป็นต้น ซึ่งเหล่านี้คือข้อกำหนดความปลอดภัยและคุณภาพของเดกซ์แทรน เช่นกัน
กิตติกรรมประกาศ
ผู้วิจัยขอขอบคุณสำนักเครื่องมือวิทยาศาสตร์และการทดสอบ ที่ให้การสนับสนุนอุปกรณ์ สารเคมี เครื่องมือและอาคารสถานที่ ในการวิจัย จึงขอขอบคุณมา ณ โอกาสนี้
การใช้ปัญญาประดิษฐ์ (Generative AI) ในงานเขียนเชิงวิชาการ
ผู้วิจัยได้ประยุกต์ใช้ปัญญาประดิษฐ์ประเภท Generative AI คือ เพื่อใช้ในการสืบค้นข้อมูลที่เกี่ยวข้องกับการวิจัย ผู้วิจัยได้ดําเนินการตรวจสอบความถูกต้อง ความครบถ้วน และความน่าเชื่อถือของข้อมูลจากแหล่งอ้างอิงก่อนนํามาใช้ประกอบการจัดทําบทความ และใช้ ChatGPT ในการตรวจสอบความถูกต้องของการใช้ภาษาและการจัดรูปแบบ โดยการใช้เครื่องมือดังกล่าวอยู่ภายใต้การกํากับดูแลและการควบคุมของผู้วิจัย
คำชี้แจงบทบาทผู้เขียน (CRediT Author Statement)
ศักรินทร์ วรรณวงศ์: การวางแนวคิด; ระเบียบวิธีวิจัย; การจัดการและดูแลข้อมูล; การดําเนินการวิจัย; การเขียนร่างต้นฉบับ; การทบทวนและแก้ไขต้นฉบับ
เอกสารอ้างอิง
นิภาภรณ์ ลักษณ์สมยา และ จินตนา กิจเจริญวงศ์. (2558). การประเมินความถูกต้องของวิธีวิเคราะห์โปรตีนในผลิตภัณฑ์ปรุงรสที่ได้จากการย่อยโปรตีนของถั่วเหลือง โดยการเปรียบเทียบผลระหว่างห้องปฏิบัติการที่มีความเชี่ยวชาญ. วารสารกรมวิทยาศาสตร์การแพทย์, 57, 54-71.
American Public Health Association, American Water Works Association, & Water Environment Federation. (2017). Standard methods for the examination of water and wastewater (23rd ed.). Washington, DC: American Public Health Association.
AOAC International. (2023). Official methods of analysis of AOAC International (22nd ed.). Rockville, MD: AOAC International.
AOAC International. (2023). Appendix F: Guidelines for standard method performance requirements. Rockville, MD: AOAC International.
ASTM International. (2007). Standard test method for total nitrogen in organic materials by the Kjeldahl method (ASTM E258-07). West Conshohocken, PA: ASTM International.
Balarajah, T., Niroshan, A., Chem, M. I., & Udagedara, D. T. (2025), Validation of the Kjeldahl method for total Kjeldahl nitrogen analysis in Dry Aru Reservoir, Kilinochchi, Sri Lanka (pp. 443-452). In Proceedings of the International Water Conference 2025. Colombo, Sri Lanka.
Beljkaš, B., Matić, J., Milovanović, I., Jovanov, P., Mišan, A., & Šarić, L. (2010). Rapid method for determination of protein content in cereals and oilseeds: validation, measurement uncertainty and comparison with the Kjeldahl method. Accreditation and Quality Assurance, 15(10), 555-561.
Bi, Q., Hong, T., Mei, X., Xu, X., & Xu, D. (2023). Effect of high-molecular weight dextran-enriched sourdough fermented using Leuconostoc mesenteroides ATCC 8293 on bread quality and gluten. Food Bioscience, 53, 102777.
Cantwell, H. (2025). The fitness for purpose of analytical methods: A laboratory guide to method validation and related topics (3rd ed.). Retrieved from https://www.eurachem.org/images/stories/Guides/pdf/MV_guide_3rd_ed_V1_EN.pdf
Cheng, Y., Tang, W., Xu, Z., Wen, L., & Chen, M. (2017). Structure and functional properties of rice protein–dextran conjugates prepared by the Maillard reaction. International Journal of Food Science & Technology. 53(2), 372-380.
Cote, G., & Willet, J. (1999). Thermomechanical depolymerization of dextran. Carbohydrate Polymers, 39(2), 119-126.
Díaz-Montes, E. (2021). Dextran: Sources, structures and properties. Polysaccharides, 2(3), 554-565
Dingman, R., & Balu-Iyer, S. V. (2019). Immunogenicity of protein pharmaceuticals. Journal of Pharmaceutical Sciences, 105, 1637-1654.
International Conference on Harmonisation of Technical Requirements for Registration of Pharmaceuticals for Human Use. (2005). Validation of analytical procedures: Text and methodology Q2(R1). Geneva, Switzerland: ICH Steering Committee.
Islam, M. A., & Islam, S. (2024). Sourdough bread quality: Facts and factors. Foods, 13(13), 2132.
Kitpakornsanti, K., Pengthamkeerati, P., Worachananant, P., & Limsakul, A. (2022). Soil nitrogen stock of primary and restored mangrove forests in ranong biosphere reserve, Thailand. Journal of Fisheries and Environment, 46(3), 108-118.
Koirala, P., Maina, N. H., Nihtilä, H., Katina, K., & Coda, R. (2021). Brewers’ spent grain as substrate for dextran biosynthesis by Leuconostoc pseudomesenteroides DSM20193 and Weissella confusa A16. Microbial Cell Factories, 20(1), 23.
Langyan, S., Bhardwaj, R., Radhamani, J., Yadav, R., Gautam, R. K., Kalia, S., & Kumar, A. (2022). A quick analysis method for protein quantification in oilseed crops: A comparison with standard protocol. Frontiers in Nutrition, 9, 892695.
Lanvers, P., Broeker, J., & Schmid, J. (2025). Clinical-type dextran: A review on process and enzyme engineering strategies to control molecular weight distribution. Carbohydrate Polymers, 364, 123783.
Lin, Y., & Chen, M. (2024). Dextran-40 reduces partial flap failure: A systematic review and meta-analysis for antithrombotics after free flaps. Plastic & Reconstructive Surgery Global Open, 12(5), 5812.
Marcó, A. (2002). Comparison of the Kjeldahl method and a combustion method for total nitrogen determination in animal feed. Talanta, 57(5), 1019-1026.
Martwiset, S., Koh, A. E., & Chen, W. (2006). Nonfouling characteristics of Dextran-containing surfaces. Langmuir, 22(19), 8192-8196.
Miao, K. H., & Guthmiller, K. B. (2025). Dextran. Retrieved from https://www.ncbi.nlm.nih.gov/books/NBK557631
Ministry of Health, Labour and Welfare. (2016). The Japanese pharmacopoeia (17th ed.). Tokyo, Japan: Ministry of Health, Labour and Welfare.
Oliverio, R., Liberelle, B., Patenaude, V., Moreau, V., Thomas E., Virgilio, N., Banquy, X., & Crescenzo, D. G. (2024). Cofunctionalization of macroporous dextran hydrogels with adhesive peptides and growth factors enables vascular spheroid sprouting. ACS Biomaterials Science & Engineering, 10(8), 5080-5093.
Petrovici, A. R., Pinteala, M., & Simionescu, N. (2023). Dextran formulations as effective delivery systems of therapeutic agents. Molecules, 28(3), 1086.
Pramudito, T. E., Desai, K., Voigt, C., Smid, E. J., & Schols, H. A. (2023). Dextran and levan exopolysaccharides from tempeh-associated lactic acid bacteria with bioactivity against enterotoxigenic Escherichia coli (ETEC). Carbohydrate Polymers, 328, 121700.
Preesong, J., Phromnak, P., Paenklang, F., Thammanatsakun, V., & Yampracha, S. (2025). Comparative study of nitrogen release from compound fertilizers in silty loam and sandy loam soils. International Journal of Agricultural Technology, 21(6), 2523-2538.
Sáez-Plaza, P., Navas, M. J., Wybraniec, S., Michałowski, T., & Asuero, A. G. (2013). An overview of the Kjeldahl method of nitrogen determination. Part II. Sample preparation, working scale, instrumental finish, and quality control. Critical Reviews in Analytical Chemistry, 43(4), 224-272.
Shintaro, N., Hakoda, A., Sakaida, K., Suzuki, T., & Yasui, A. (2005). Method performance study of the determination of total nitrogen in soy sauce by Kjeldahl method. The Japan Society for Analytical Chemistry, 21, 1129-1132.
Tarr, H. L. A., & Hibbert, H. (1931). Studies on reactions relating to carbohydrates and polysaccharides. XXXV. polysaccharide synthesis by the action of acetobacter xylinus on carbohydrates and related compounds. Canadian Journal of Research, 4(4), 372-388.
Thompson, M., Owen, L., Wilkinson, K., Wood, R., & Damant, A. (2002). A comparison of the Kjeldahl and Dumas methods for the determination of protein in foods, using data from a proficiency testing scheme. The Analyst, 127(12), 1666-1668.
Verhoef, R., Waard, D. P., Schols, H. A., Rättö, M., Siika-Aho, M., & Voragen, A. G. (2002). Structural elucidation of the EPS of slime producing Brevundimonas vesicularis sp. isolated from a paper machine. Carbohydrate Research, 337(20), 1821-1831.
Vitte, J., Vibhushan, S., Bratti, M., Montero-Hernandez, J., E., & Blank, U. (2022). Allergy, anaphylaxis, and nonallergic hypersensitivity: IgE, mast cells, and beyond. Medical Principles and Practice, 31, 501-515.
Wang, H., Pampati, N., McCormick, W., M., & Bhattacharyya, L. (2016). Protein nitrogen determination by Kjeldahl digestion and Ion chromatography. Journal of Pharmaceutical Sciences, 105, 1851-1857.